一、简介
软组织肉瘤 (Soft Tissue Sarcoma) 是一类起源于肌肉、脂肪、纤维组织、神经鞘、血管等间充质组织的恶性肿瘤,约占成人实体瘤的1%,但在儿童中占比可达15%~20%,其中以横纹肌肉瘤最为常见,占儿童病例的40%~50%。虽然总体发病率较低,但其组织学亚型多样、生物学行为差异显著,临床诊治具有高度异质性。
根据最新版世界卫生组织 (WHO) 分类,软组织肿瘤被细分为100余种良恶性类型,其中肉瘤类约80种。新分类体系在传统组织学基础上引入分子特征,强调“分子谱系”在诊断与分类中的指导作用。常见谱系包括脂肪细胞性、纤维/肌纤维母细胞性、平滑肌性、横纹肌性、血管性和神经鞘性等,同时设有“未分化”及“不确定分化”类别,以涵盖未能归入明确谱系但具有恶性行为的肿瘤[1]。例如,滑膜肉瘤中SS18-SSX融合基因的检测可提供明确诊断依据,而NTRK融合基因的发现不仅有助于肿瘤分类,也为靶向治疗开辟了新路径,凸显分子病理在现代诊断与治疗决策中的双重核心地位。
软组织肉瘤相对少见,占所有恶性肿瘤的约1%,每年全球新发病例约为10万例。其发病率约为每百万人中2-4例。可以发生在任何年龄段,但多见于中老年人,特别是在50-70岁之间。儿童和青少年中也有部分亚型 (如横纹肌肉瘤) 发生。无明显性别偏好,但某些亚型 (如滑膜肉瘤) 在男性中稍多见。在不同地区和种族中发病率差异不大,但某些亚型 (如脂肪肉瘤) 在西方国家报道较多。
临床上,最常见的表现,通常为无痛的硬性肿块,逐渐增大。肿块可以在皮下、深部组织或筋膜层中。当肿瘤压迫附近的神经或血管,或侵入骨骼时,可出现疼痛。发生在四肢或关节附近时,可能限制关节运动。肿块表面可能出现皮肤变色、发红或溃破 (少见) 。
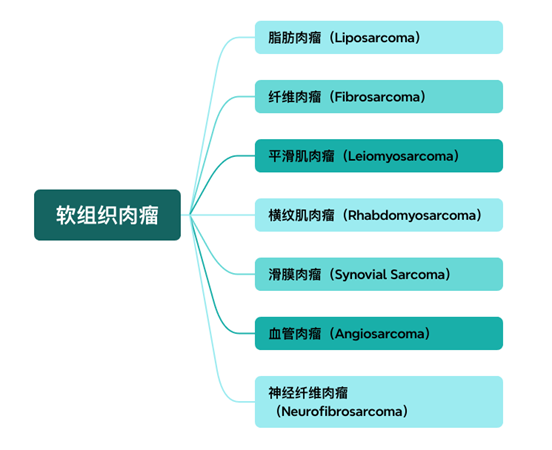
图1 软组织肉瘤的分类
二、检测与诊断
软组织肉瘤在早期常表现为局部无痛性肿块,肿瘤通常生长缓慢,不引起明显功能障碍,因此易被忽视或误诊为良性病变。当病灶逐渐增大至压迫邻近神经或血管结构时,患者才常因疼痛、麻木或功能受限等症状前来就诊。
影像学评估在软组织肉瘤的初筛、分期以及手术可切除性判断中起到关键作用。磁共振成像 (MRI) 因其在显示肿瘤边界、内部结构、与邻近组织关系及血供情况方面的高分辨率,被认为是评估软组织肿瘤的首选影像手段,尤其适用于四肢、盆腔或躯干深部病灶。计算机断层扫描 (CT) 在肺部远处转移的评估中具有重要地位,是确诊期及随访期间不可或缺的检查方法。正电子发射断层扫描 (PET-CT) 则对代谢活跃或疑似远处转移的肉瘤亚型具有补充价值,不仅有助于原发灶和转移灶的识别,也在治疗应答监测和复发评估中发挥作用[2]。不同成像方式间的协同应用可提高诊断的全面性和准确性,在治疗路径选择中也具有参考价值。
明确诊断需依赖病理组织学活检,其中粗针穿刺活检 (core needle biopsy) 因能够获取足量组织样本支持组织学分型,被广泛推荐作为首选方式。相比之下,细针抽吸 (fine needle aspiration) 因组织结构信息不足,不宜用于初始诊断。组织学诊断常需结合免疫组化与分子遗传学分析。免疫组化标志物,如S-100、Desmin、Myogenin、CD34、CD31等,能辅助识别肿瘤来源。在分子层面,多个软组织肉瘤亚型具有特征性染色体易位与融合基因,如EWSR1-FLI1见于尤文肉瘤,SS18-SSX为滑膜肉瘤特有,FUS-DDIT3则可提示黏液样脂肪肉瘤。这些分子改变不仅提高了亚型分类的准确性,也为个体化治疗提供了潜在靶点[3]。
需要指出的是,软组织肿瘤的组织学类型复杂,诊断难度较大,误诊率不可忽视。对英国一所转诊中心10年间的软组织肿瘤病理资料 (Thway et al., 2009) 进行回顾性分析发现,约10.9%的病例在由基层医院转入专科中心后被重新诊断为另一肿瘤类型,这些修正对治疗决策产生实质性影响。
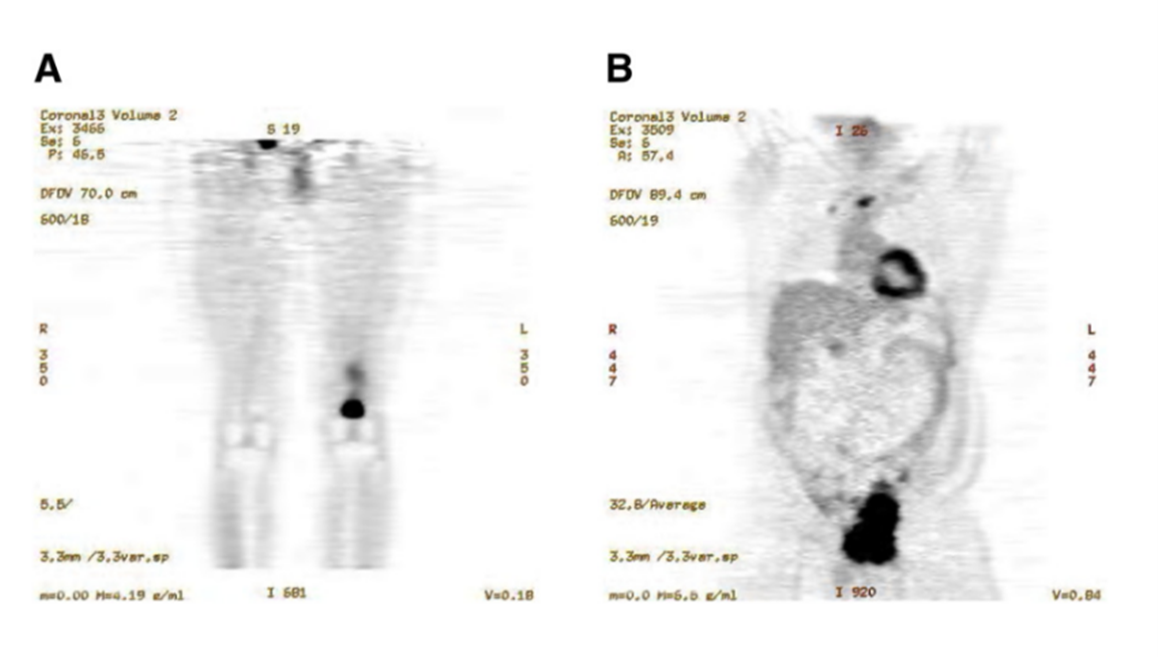
图2 原发性肉瘤肿瘤患者的18F-FDG PET 图像。 (A) 左侧股骨骨平滑肌瘤患者的冠状面图像。 (B) 右侧骨盆血管肉瘤患者的冠状面图像。
三、风险与预防
软组织肉瘤的确切发病机制尚不完全明确,现有研究已识别出多种内源性和外源性风险因素。既往接受高剂量放射治疗的患者,其发病风险显著升高,尤其是乳腺癌、霍奇金淋巴瘤等治疗史患者。部分肉瘤与遗传性疾病密切相关,如Li-Fraumeni综合征 (TP53基因突变) 、神经纤维瘤病I型 (NF1突变) 、家族性腺瘤性息肉病 (APC突变) 等,携带这些基因突变的个体罹患软组织肉瘤的风险明显高于常人。此外,一些亚型肉瘤可通过特定染色体易位被明确识别,例如滑膜肉瘤中t(X;18)(p11;q11)易位导致SS18-SSX融合基因,横纹肌肉瘤中PAX3-FOXO1融合基因等,这些分子事件不仅在发病机制中具有关键作用,也常被用作诊断和预后标志物。
环境因素方面,氯乙烯、二恶英、苯胺染料等工业化学品暴露、慢性淋巴水肿、异物植入 (如义体材料) 均被报道与个别亚型软组织肉瘤相关[4]。目前尚无针对该类肿瘤的有效一级预防措施。医学界建议对高危人群 (如有家族遗传病史者、既往接受过放疗者) 加强随访,重视影像学筛查和临床症状识别,以期早期发现、早期干预。
四、治疗方案
软组织肉瘤的治疗策略依赖多学科团队 (MDT) 制定,需综合评估肿瘤的大小、部位、组织学分级、转移状态,以及患者的年龄与功能状态。对局限性病变,根治性手术为首选治疗方式,目标为“广泛切除”,即在最大限度保留功能的前提下完整切除病灶及其潜在浸润组织,力求获得阴性切缘。根据NCCN和ESMO指南,高分级 (G2/G3) 或切缘阳性、解剖位置复杂 (如骨盆、腘窝) 者术后推荐辅以放疗,以降低局部复发风险[5]。
对于肿瘤体积大、边界模糊或邻近重要结构的患者,可行术前新辅助放疗或化疗以缩小病灶、提高手术可行性与完整性。对于晚期或转移性软组织肉瘤,系统性治疗仍以化疗为主,其中阿霉素联合异环磷酰胺是目前一线推荐方案,在未分化肉瘤、滑膜肉瘤等中具有一定活性。但总体客观缓解率有限,且毒副作用不容忽视。对于部分低危患者 (如分化良好、进展缓慢的脂肪肉瘤) ,可根据个体情况选择单药阿霉素治疗。
少数亚型肉瘤携带明确分子靶点,可从靶向治疗中获益。例如,胃肠道间质瘤 (GIST) 中KIT或PDGFRA突变患者对伊马替尼高度敏感,已成为标准治疗模式。其他亚型如MDM2扩增的黏液样脂肪肉瘤对CDK4抑制剂 (如Palbociclib) 在II期试验中显示一定疗效,但尚未纳入标准治疗;NTRK融合基因在软组织肉瘤中的阳性率不足1%,相关靶向药物 (Larotrectinib、Entrectinib) 虽已获批,但仅适用于极少数患者[6]。
免疫治疗在软组织肉瘤中的总体应答率仍有限,主要集中于肺泡状软组织肉瘤、去分化脂肪肉瘤等PD-L1表达较高的亚型。既往研究显示其客观缓解率约为10%~15%,仍需更多前瞻性临床试验验证疗效及预测标志物。当前正探索PD-1/PD-L1抑制剂与低剂量化疗、靶向药物或放疗的联合方案,以期增强免疫应答[7]。
治疗后的随访管理对于预后具有关键意义。接受根治性治疗的患者需定期随访,包括局部MRI和胸部CT检查,用于监测复发与远处转移。随访频率通常依据复发风险分级确定,前两年建议每3–6个月一次,第三年至第五年每6–12个月一次,五年后可逐步延长间隔。对于四肢病灶术后患者,应尽早进行功能康复训练,以预防残疾和改善生活质量。
参考文献
[1] WHO Classification of Tumours Editorial Board. Soft Tissue and Bone Tumours. WHO Classification of Tumours, 5th Edition, Volume 3. Lyon (France): International Agency for Research on Cancer; 2020.
[2] Eary JF, Conrad EU. Imaging in sarcoma. J Nucl Med. 2011;52(12):1903–1913.
[3] Thway K, Fisher C. Histopathological diagnostic discrepancies in soft tissue tumours referred to a specialist centre: reappraisal after histopathological review. Sarcoma. 2009;2009:1–7.
[4] Burningham Z, Hashibe M, Spector L, et al. The epidemiology of sarcoma. Clin Sarcoma Res. 2012;2:14.
[5] O’Sullivan B, Davis AM, Turcotte R, et al. Preoperative versus postoperative radiotherapy in soft-tissue sarcoma of the limbs: a randomized trial. Lancet. 2002;359(9325):2235–2241.
[6] Demetri GD, von Mehren M, Blanke CD, et al. Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med. 2002;347(7):472–480.
[7] Banks, L. B., & D’Angelo, S. P. (2022). The Role of Immunotherapy in the Management of Soft Tissue Sarcomas: Current Landscape and Future Outlook. Journal of the National Comprehensive Cancer Network, 20(7), 834-844. Retrieved May 9, 2025, from https://doi.org/10.6004/jnccn.2022.7027


