- 简介
肾细胞癌(Renal-cell carcinoma,RCC)是起源于肾小管上皮的恶性肿瘤,是泌尿系统较常见的肿瘤之一。根据国际癌症研究机构发布的GLOBOCAN最新统计,2022年全球新增RCC病例约43万例,居恶性肿瘤第14位,低于泌尿系统的前列腺癌及膀胱癌,死亡率居第16位,占所有癌症新发病例的2.2%1。近年来,在大多数国家和地区,肾癌的发病率都呈逐年上升的趋势,且男性的发病率高于女性。肾细胞癌年龄标准化发病率在男性为6.1/10万,女性为3.2/10万。年龄标准化死亡率在男性为4.6/10万,女性为1.8/10万。
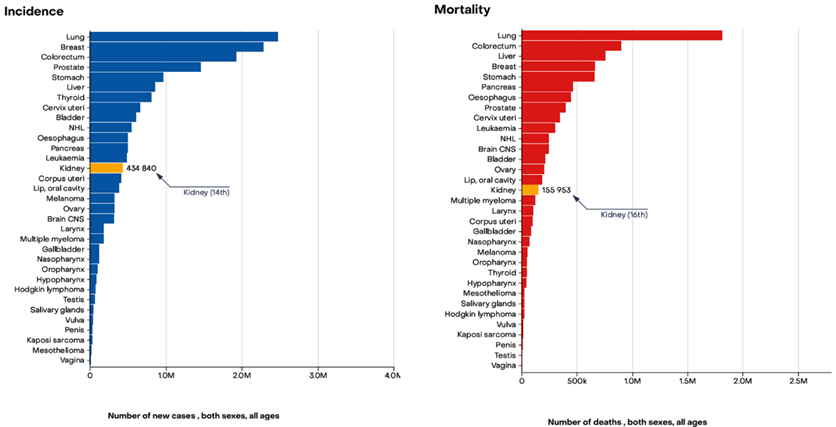
图1. 2022年全球肾癌发病率和死亡率。
肾脏是我们身体不可或缺的一部分,失去肾脏可能会导致尿毒症、电解质紊乱、高血压等并发症,严重降低生活质量。肾细胞癌通常在肾脏内部形成,早期可能没有任何症状,因此很难被发现。典型的肾细胞癌三联征为:血尿、腰痛、腹部肿块,如果有三种症状中的一种或两种,应当有所警惕。间歇无痛肉眼血尿为常见症状,表明肿瘤已侵入肾盏、肾盂。疼痛常为腰部钝痛或隐痛,血块通过输尿管时可发生肾绞痛。肿瘤较大时在腹部或腰部易被触及。副瘤综合征又称肾外表现,常见有高血压、贫血、体重减轻、恶病质、发热、红细胞增多症、肝功能异常、高钙血症、高血糖、红细胞沉降率增快、凝血机制异常等。同侧阴囊内可发现精索静脉曲张,平卧位时不消失,提示肾静脉或下腔静脉癌栓形成。如出现转移,还可有一些特征性表现,如肺转移出现咳嗽、咯血,骨转移出现骨痛、骨折,脑转移出现头痛,淋巴结转移有颈部肿块等。
- 肾细胞癌的病理分类及分级系统
绝大多数肾细胞癌发生于一侧肾脏,双侧肾细胞癌(异时或同时)仅占散发性肾细胞癌的2%~4%。肾肿瘤常为单发肿瘤,其中10%~20%为多发病灶。多发病灶病例常见于遗传性肾细胞癌以及乳头状肾细胞癌的患者。肿瘤瘤体大小差异较大,常有假包膜与周围肾组织相隔。RCC起源于肾实质,特别是来自肾单位的细胞,可以进一步分为组织学亚型。肾细胞癌的组织病理类型最常见的为透明细胞癌(ccRCC),起源于近端肾小管上皮细胞(PTEC),其次为乳头状肾细胞癌及嫌色细胞癌,以及集合管癌等少见类型的肾细胞癌2。
人ccRCC的多项基因组研究显示,编码VHL(von Hippel-Lindau 抑癌基因)的3p染色体3p存在完全或部分双等位基因缺失3。染色体3p的缺失归因于染色体裂解错误,在正常PTEC的有丝分裂过程中形成微核,正常PTEC中微核形成的触发因素归因于它们对低氧微环境的敏感性,这是ccRCC进展的一个标志。VHL表达的改变存在于80%–93%的原发性 ccRCC病例中,形成自我延续的缺氧PTEC微环境。PTEC是ccRCC中的起源细胞,在缺氧条件下从正常状态转变为恶性状态。在获得额外的基因改变后,PTEC从正常(图2,步骤1)到前体VHL+/-(图2,步骤2),最后是恶性VHL-/-(图2,步骤3)。一旦PTEC转变为恶性状态,他们就会在肾脏内形成原发性ccRCC(图2,步骤3.a)病变或局部侵袭性ccRCC(图2,步骤3.b)病变,这些病变延伸到邻近的大血管和/或转移性ccRCC(图2,步骤3.c)病变扩散到远处器官4。
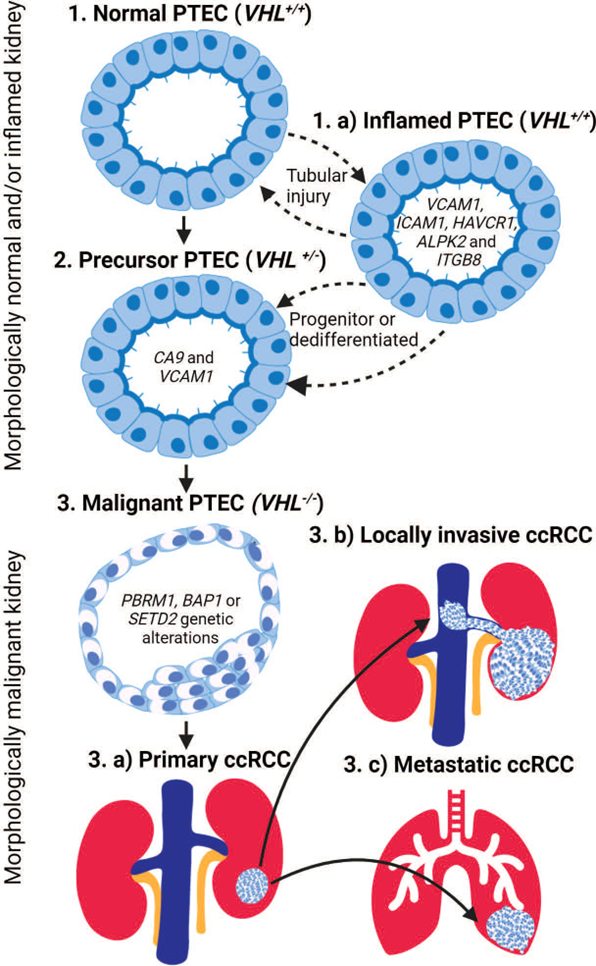
图2. 近端肾小管上皮细胞(PTEC)在ccRCC发展中的转变。
表1. 2016年WHO肾细胞肿瘤病理组织学分类及特征。
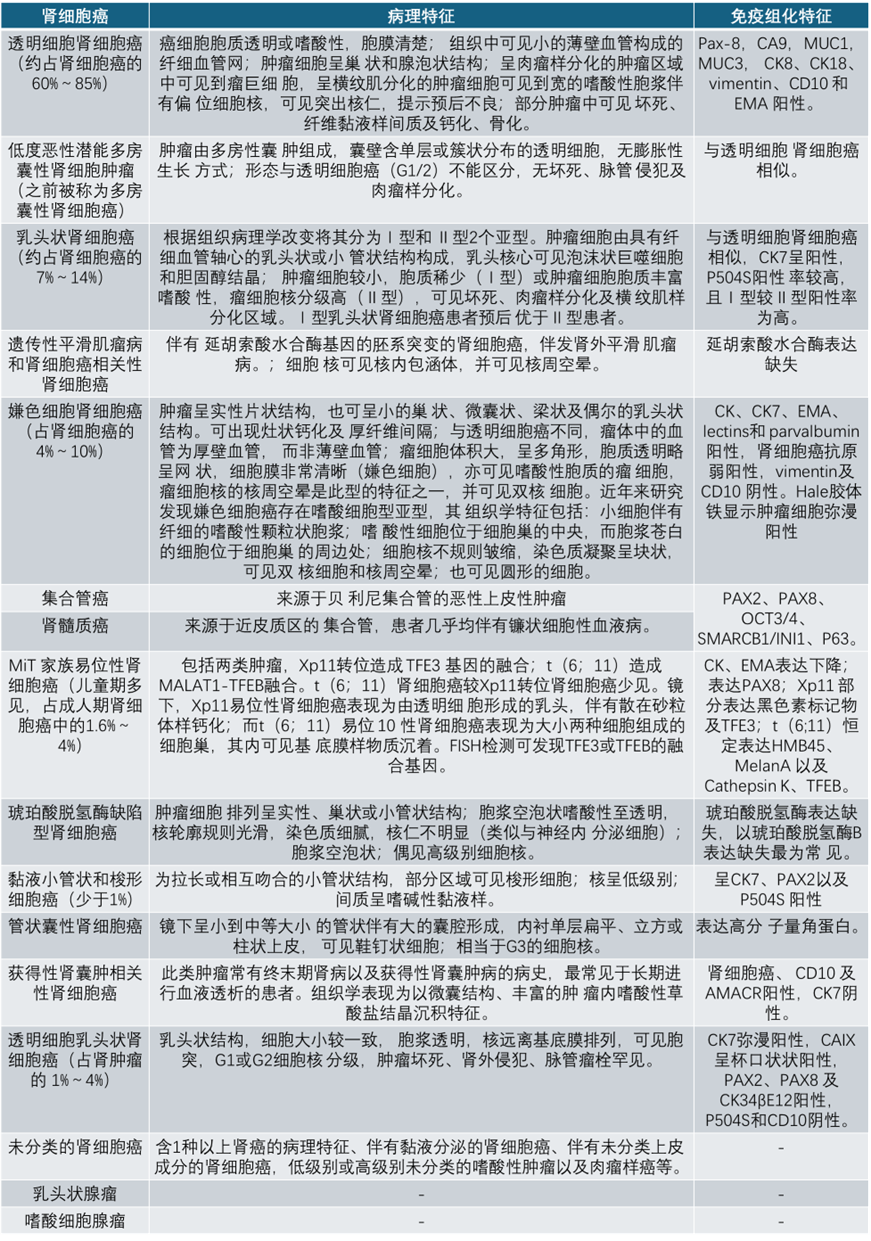
病理分级是一个重要的预后相关因素,只适用于透明细胞肾细胞癌和乳头状肾细胞癌。
表2. 2016版肾细胞癌WHO/ISUP核分级标准。

- 检测与诊断5
肾癌的诊断主要依靠临床表现、实验室检查和影像学检查。
从病史和症状的角度,多数肾脏小肿瘤均没有临床表现,多在体检时发现。肾肿瘤较大时腰部或腹部可触及肿块,部分可伴有腰部叩痛。
实验室常规检查的目的是了解患者的一般状况以及是否适于采取相应的治疗措施,主要包括尿常规、血常规、红细胞沉降率、血糖、血钙、肾功能(血尿素氮、血肌酐和肾小球滤过率)、肝功能、乳酸脱氢酶、碱性磷酸酶等项目。以上项目的检查结果在肾细胞癌患者中可表现为血尿、红细胞增多、贫血、红细胞沉降率增快、高血糖、高血钙、肾功能异常及肝功能异常等。目前,尚无公认的用于肾细胞癌早期辅助诊断的血清肿瘤标志物。
胸部X线检查,肾细胞癌患者应常规行胸部正侧位X线片,对胸部X线片有可疑结节或临床分期≥Ⅲ期的患者,需做胸部CT。
腹部超声检查是发现肾肿瘤最简便和常用的方法。肾超声造影检查有助于鉴别肾肿瘤良恶性,适用于慢性肾功能衰竭或碘过敏而不适宜行增强CT扫描的肾肿瘤患者以及复杂性肾囊肿患者的鉴别诊断。
腹部CT检查是肾细胞癌术前诊断及术后随访的最常用检查方法。完整CT检查应包括平扫和多期增强扫描。CT扫描可对大多数肾肿瘤进行定性诊断,具有较高的诊断敏感性和特异性,是术前临床分期的重要依据。而对于造影剂过敏、妊娠及担心辐射的年轻患者,可选择磁共振来替代增强CT。MRI对肾细胞癌诊断的敏感性和特异性等 于或略高于CT。
核素肾动态显像能准确评价肾细胞癌患者术前双肾和分肾功能,有助于指导手术方案的决策。
经皮肾穿刺活检包括空芯针活检和细针吸取(fine-needle aspiration,FNA),能为影像学不能诊断的肾肿瘤提供病理组织学依据。
- 风险与预防
病因分析
肾细胞癌的病因尚不明确,其发病与遗传、吸烟、肥胖和高血压等有关6。
大部分肾细胞癌是散发性的,遗传性肾细胞癌占肾细胞癌总数的2%~4%,多以常染色体显性遗传方式在家族中遗传,由不同的遗传基因变异造成,这些基因既包括抑癌基因又包括癌基因。某些家族遗传综合征患者,如患希佩尔-林道综合征(Von Hippel-Lindau病,VHL病)、Birt-Hogg-Dube综合征、结节性硬化症等家族遗传患者,会增加肾癌的发生风险。
吸烟可以增加患肾细胞癌的危险,前瞻性研究认为吸烟是中等度危险因素。既往有吸烟史的人患肾细胞癌的相对危险度为1.3,而正在吸烟的人患肾细胞癌的相对危险度为1.6。
肥胖程度一般用体重指数来表示,体重指数增加,则患肾细胞癌的危险性增加。肥胖增加肾细胞癌风险的具体机制未明,可能和肥胖增加雄性激素及雌性激素释放,或者与脂肪细胞释放的一些细胞因子相关。
与普通人相比有终末期肾病患者的肾细胞癌发病率更高。长期透析的患者容易患获得性肾囊肿7。在这些肾细胞癌患者中,肿瘤通常是双侧、多发的,组织学上呈现乳头状结构。
有证据表明,饮酒、职业暴露于三氯乙烯、高雌激素的女性等都有可能增加患肾细胞癌的风险6。尚需要进一步研究遗传因素与环境暴露之间相互作用的潜在影响。
预防措施
肾细胞癌的发病原因尚未完全明确,因此没有确切的可预防肾细胞癌发生的措施。但目前认为肾细胞癌的发生与多种因素有关,因此有一些预防肾细胞癌发生的建议:
- 生活方式调整:包括戒烟、控制体重、健康饮食、限制饮酒、多运动等。
- 管理慢性疾病:包括控制血压、控制血糖、控制血脂等。
- 避免职业暴露:避免接触砷、石棉、镉等有害化学物质。
- 定期体检:早期发现的肾癌往往预后较好,患者的生存期都很长,定期进行体检和筛查对于早期发现肾癌非常关键。建议每年行一次常规健康体检,应当包含尿常规以及肾脏超声或腹部平扫CT检查。有肾癌家族史以及高风险因素(吸烟、肥胖和高血压)人群应从40岁左右开始定期筛查。如有发现任何异常结果,建议进行腹部增强CT或者磁共振等检查进一步明确诊断。
- 治疗方案8,9
肾细胞癌患者通过影像学检查结果确定肿瘤的临床分期,利用辅助检查评估患者对治疗的耐受能力,根据临床分期并结合患者的耐受力,选择恰当的治疗方式。对于局限性肾癌、局部进展性肾癌,以手术治疗为主,手术方式包括肾部分切除术和根治性肾切除术。对手术的患者依据病理学检查结果确定病理分期,根据病理分期选择术后治疗及随诊方案。术后需定期随访以防复发。
如果确诊为肾癌,医生会根据临床分期,身体状况,从而制定相应的个体化治疗方案。
(一)手术治疗
手术治疗是局限性(I、II期)和局部进展期(III期)肾癌首选治疗方法。局限性肾癌患者通过手术可获得治愈,局部进展期患者术后存在复发可能,需要进行辅助治疗。
(1)肾部分切除术。切除含有肿瘤部分正常肾组织,它适用于直径<4cm肿瘤患者,可以保护患者肾功能,减少术后心血管疾病发生风险。
(2)根治性肾切除术。切除包括肿瘤在内的整个肾脏和肾周围组织如脂肪、部分输尿管等。适用于无法行肾部分切除术或肿瘤直径>7cm、局部进展期肾癌患者。
(二)非手术疗法
小体积肾癌或身体无法耐受手术患者可通过非手术疗法进行治疗。
(1)冷冻消融。在B超或腔镜引导下,将特殊的空心针经皮插入肾肿瘤内部,通过快速降温破坏癌细胞,引起细胞坏死或凋亡。
(2)射频消融。在B超或腔镜引导下,将电极经皮肤插入肾肿瘤内部,通过射频高能量产生高温,导致细胞变性,坏死。
(三)药物治疗
药物治疗可用于:转移性或晚期肾癌(IV期);无法手术治疗患者,肾癌术后复发患者;局部进展期患者术后辅助治疗。
(1)靶向药物治疗。对于晚期肾癌,靶向药物治疗已成为重要的治疗手段。它通过精准作用于肿瘤细胞的特定靶点,阻断肿瘤血管生成和细胞增殖,从而抑制肿瘤生长,达到治疗目的。
(2)免疫治疗。免疫治疗通过激活患者自身的免疫系统来攻击肿瘤细胞,有助于有效地识别和杀灭癌细胞。免疫治疗可以作为一种单独治疗或与靶向药物联合治疗。
其他治疗:对于无法手术切除或术后复发转移的肾癌患者,还可根据具体情况选择放疗、化疗、介入治疗等,以缓解症状,延长生存期。
参考文献
1 Sun, S. et al. Current perspectives and trends in nanoparticle drug delivery systems in breast cancer: bibliometric analysis and review. Front Bioeng Biotechnol 11, 1253048 (2023). https://doi.org/10.3389/fbioe.2023.1253048
2 Chow, W. H., Dong, L. M. & Devesa, S. S. Epidemiology and risk factors for kidney cancer. Nat Rev Urol 7, 245-257 (2010). https://doi.org/10.1038/nrurol.2010.46
3 Chen, F. et al. Multilevel Genomics-Based Taxonomy of Renal Cell Carcinoma. Cell Rep 14, 2476-2489 (2016). https://doi.org/10.1016/j.celrep.2016.02.024
4 Raghubar, A. M. et al. Cellular milieu in clear cell renal cell carcinoma. Front Oncol 12, 943583 (2022). https://doi.org/10.3389/fonc.2022.943583
5 Vogel, C. et al. Imaging in Suspected Renal-Cell Carcinoma: Systematic Review. Clin Genitourin Cancer 17, e345-e355 (2019). https://doi.org/10.1016/j.clgc.2018.07.024
6 Kabaria, R., Klaassen, Z. & Terris, M. K. Renal cell carcinoma: links and risks. Int J Nephrol Renovasc Dis 9, 45-52 (2016). https://doi.org/10.2147/ijnrd.S75916
7 Heinz-Peer, G., Schoder, M., Rand, T., Mayer, G. & Mostbeck, G. H. Prevalence of acquired cystic kidney disease and tumors in native kidneys of renal transplant recipients: a prospective US study. Radiology 195, 667-671 (1995). https://doi.org/10.1148/radiology.195.3.7753991
8 Posadas, E. M. & Figlin, R. A. Systemic therapy in renal cell carcinoma: advancing paradigms. Oncology (Williston Park) 26, 290-301 (2012).
9 Grigolo, S. & Filgueira, L. Immunotherapy of Clear-Cell Renal-Cell Carcinoma. Cancers (Basel) 16 (2024). https://doi.org/10.3390/cancers16112092


