一、皮肤癌简介
皮肤癌(Skin cancer,SC)是皮肤细胞异常增殖形成的恶性肿瘤,主要诱因包括长期紫外线暴露、化学致癌物接触、遗传因素及免疫抑制等。根据病理类型,皮肤癌可分为非黑色素瘤(如基底细胞癌、鳞状细胞癌)和黑色素瘤两大类[1]。通常,人们更倾向于关注发病频率更高的肺癌、乳腺癌或结直肠癌,从而忽略一些早期隐蔽性更高、晚期存活率极低的肿瘤疾病,皮肤肿瘤就是其中一类,尤其是黑色素瘤。
二、全球发病率与死亡率
2.1 发病率
根据国际癌症研究机构(the International Agency for Research on Cancer,IARC)更新估算的2022年全球癌症统计数据[2],全球新增癌症病例接近2000万,癌症死亡病例达970万,大约每5个人中就有一人在一生中会患上癌症,而大约每9个男性中有1人、每12个女性中有1人会死于癌症。其中,2022年全球皮肤癌新增病例约156.5万例,其中非黑色素瘤占95%(约123.5万例),黑色素瘤占5%(约33.2万例)。
- 排名:从新增病例数看,非黑色素瘤皮肤癌(Non-melanoma skin cancer,NMSC)是全球第4大常见癌症,黑色素瘤(Melanoma skin cancer,MSC)位列第17,见图1。
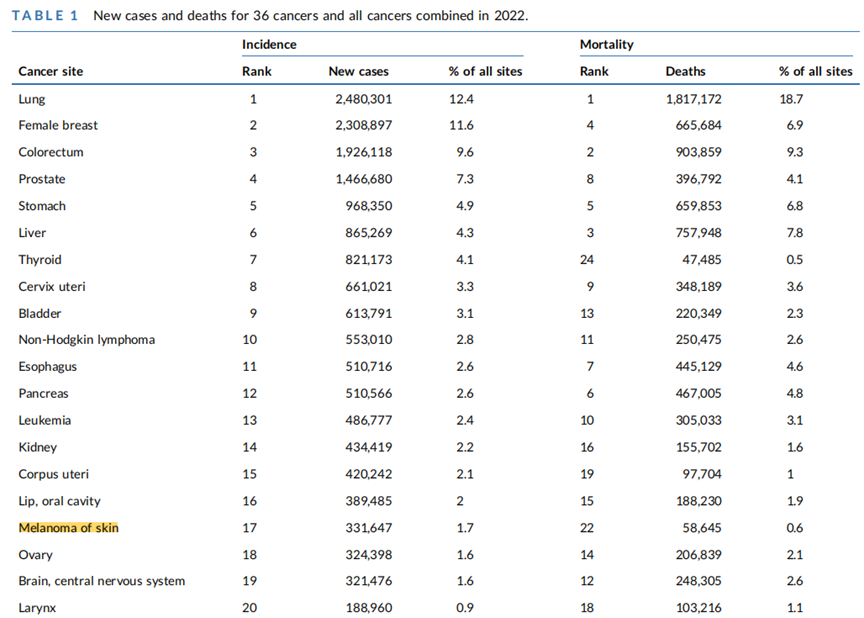
图1. 2022年全球不同癌种新增和死亡数量排名[2]。
- 地区差异:澳大利亚/新西兰发病率最高(每10万人中9例),西非最低(每10万人中97.1例);在澳大利亚或新西兰,NMSC是男性和女性中发病最高的癌种,在美国,NMSC是男性发病最高的癌种。
- 性别差异:NMSC的男性发病率普遍高于女性,男性发病率为14%,女性发病率为5%;对于MSC,男性发病率为3.7%,女性发病率为2.9%。
2.2 死亡率
2022年全球皮肤癌死亡约13.8万例,其中NMSC死亡6.9万例,MSC死亡5.8万例。尽管黑色素瘤致死率更高,但非黑色素瘤因病例基数大,总死亡人数更多。
三、皮肤癌分类、特点、病因及治疗策略
3.1 非黑色素瘤(NMSC)
NMSC可分为基底细胞癌(Basal Cell Carcinoma,BCC)和鳞状细胞癌(Squamous Cell Carcinoma,SCC)。
3.1.1 BCC
基底细胞癌(BCC)是人类最常见的皮肤恶性肿瘤类型,生长缓慢,极少转移,其最大风险因素是暴露于阳光。尽管BCC的死亡率较低,因此通常未被纳入癌症登记系统,但通过分析美国保险登记数据和官方统计,BCC的年发病率预计将达到430万例。BCC在白种人群发病率显著更高,该病死亡率虽低,但因局部组织破坏导致的高发病率令人关注。
组织学角度:BCC起源于表皮基底层的角质形成细胞,其临床表现为浅粉色或肉色珍珠样丘疹或斑片,属于侵袭性最低的皮肤癌类型,主要好发于长期暴露于紫外线的体表区域,如面部、手部、颈部、腿部和腹部。尽管多数局限生长,但可能扩散至体表其他部位或侵犯神经、骨骼。
主要致病机制:(1)长期日光暴露使得紫外线破坏DNA并削弱免疫防护;(2)免疫功能缺陷或免疫抑制;(3)β型人乳头瘤病毒(HPV);(4)人类免疫缺陷病毒(HIV)感染。
分子病理机制:聚焦于patched/hedgehog细胞内信号通路的异常激活,具体表现为PTCH1基因失活突变(70-90%病例)、SMOm基因激活突变(约10%病例)、SUFU基因功能缺失突变(小部分病例)、p53抑癌基因紫外线特异性突变(50%病例存在)。
治疗策略:以局部控制为主,包括放射治疗、局部药物治疗(如5-氟尿嘧啶)、联合治疗方案。值得注意的是,BCC具有迟发复发的特性,随机对照研究显示,手术切除后2.5年复发率为3%,10年升至12%,且56%的复发发生在术后5年以上。
3.1.2 SCC
SCC恶性程度较高,易形成红色粗糙肿块,可能转移至淋巴结。风险因素有:长期紫外线暴露、慢性炎症或免疫抑制(如器官移植患者)等。美国年新发病例约25万,白种人群一生中患SCC的风险在7-11%,其中男性患病几率在9-14%,女性为4-9%。相较基底细胞癌(BCC),CSCC具有更高侵袭性,总体死亡率0.3-3.7%,转移后生存率显著下降,淋巴结转移率约4%,致死率近2%。
组织学角度:SCC为表皮角质形成细胞异常增生,表现为鳞屑性红斑或质硬丘疹。
主要致病机制:(1)紫外线过度暴露(主要诱因);(2)皮肤光敏表型(白皙肤色易感);(3)免疫抑制状态;(4)慢性皮肤损伤(烧伤瘢痕、溃疡);(5)化学致癌物接触(如接触砷、焦油、沥青等物质);(6)年龄相关性累积损伤。
分子病理机制:初期,紫外线诱导TP53基因突变,引起基因组不稳定性;进展期,RAS等癌基因激活,CDKN2A、NOTCH等抑癌基因失活;终末期,NF-κB、MAPK、PI3K/Akt/mTOR等信号通路激活导致表皮生长因子受体(EGFR)上调。
治疗策略:手术切除为主流方案,放射治疗作为辅助手段,系统治疗方案适用于晚期病例。术后10年生存率>90%(早期病例),转移灶出现后生存率急剧下降。
3.2 黑色素瘤(MSC)
MSC最为致命,占皮肤癌死亡的75%,早期表现为不规则痣(颜色、形状变化),转移后5年生存率低于14%。
组织学角度:起源于表皮基底层黑素细胞恶性转化黑色素瘤。
主要致病机制:(1)致癌基因激活(如BRAF、NRAS突变);(2)抑癌基因失活(如CDKN2A、TP53);(3)DNA修复机制受损;(4)紫外线辐射诱导基因组不稳定性。
临床诊断标准(ABCD法则):(1)不对称性(Asymmetry),皮损两侧形态不一致;(2)边缘不规则(Border irregularity),边界呈锯齿状或地图样改变;(3)颜色异质性(Color variation),病灶呈现棕、黑、蓝、红等多色混杂;(4)直径(Diameter),通常>6mm(约铅笔橡皮大小),但存在个体差异。
临床分型与特征:(1)浅表扩散型黑色素瘤(75%),表现为原有痣样皮损出现大小、形状或颜色改变,女性好发于下肢,男性多见于躯干,水平生长期皮损呈不对称性扩展;(2) 结节型黑色素瘤(15-30%),表现为快速增生的坚硬、对称性色素性丘疹/结节,垂直生长为主,易发生溃疡及出血;(3)恶性雀斑样痣型(4-15%),高发人群为>60岁日光暴露者("老年性雀斑"),初期为边界不清的褐色斑片,缓慢增大后可突发浸润性生长,首选手术切除,次选放射治疗,无法手术者采用咪喹莫特乳膏局部治疗;(4)肢端雀斑样痣型(2-3%),掌跖、指(趾)甲床等非日光暴露部位,亚非人群为主要亚型(占该群体黑色素瘤的50-70%),早期诊断困难导致晚期就诊率高,手术需兼顾功能保留与根治性切除,术后常需皮瓣修复等重建手术,晚期患者对免疫检查点抑制剂(如PD-1单抗)和靶向治疗(BRAF/MEK抑制剂)显示出初步应答。
预后影响因素:(1)原发灶特征,关注Breslow厚度、溃疡存在、有丝分裂指数等指标;(2)转移状态,如局部转移(5年生存率25-70%)和远处转移(5年生存率<20%);(3)分子特征,例如BRAF V600E突变会影响靶向治疗响应。
四、检测与诊断方法
4.1 自我筛查(ABCDE法则)
A(Asymmetry)不对称
B(Border)边界不规则
C(Color)颜色不均
D(Diameter)直径>6mm
E(Evolution)短期内变化。
4.2 临床诊断技术
(1)皮肤镜:无创观察表皮结构,但对深层病变敏感度低。
(2)组织病理活检:诊断“金标准”,通过切片分析良恶性,但需手术取样。
- 新型技术:如基于生物阻抗谱的无创筛查,可检测深层组织病变;AI模型(如YOLOv8+ViT)结合数据增强技术,分类准确率达93%。
五、皮肤癌的风险和预防
5.1风险
根据2022年的一项报道,皮肤癌的风险因素主要可以分为两大类,可改变风险因素和不可改变风险因素。[3,4]
1.可改变因素
①长期紫外线暴露
紫外线(UV)辐射是皮肤癌的主要风险因素之一。紫外线来自自然阳光和人工来源,长时间暴露于紫外线会导致皮肤细胞损伤,增加患皮肤癌的风险。[5,6]
②免疫系统抑制
免疫系统功能被减弱的人,如器官移植后服用免疫抑制剂的人,以及有HIV患病史的人,患皮肤癌的风险增加。免疫系统有助于识别和摧毁癌细胞,因此其功能减弱会增加癌症风险。[7,8]
③化学物质接触
许多化学致癌物:如砷、杀虫剂、氡、硒等都属于可以诱发皮肤癌的可变风险,经常接触这些化学致癌物的人会更容易患皮肤癌。[9-11]
(arsenic, insecticides, radon, selenium)
2.不可改变因素
①皮肤类型
皮肤较白、头发较浅和眼睛颜色较浅(蓝或绿)的人更容易患皮肤癌。这种风险与皮肤中的黑色素含量有关,黑色素是一种天然的防晒色素。[12]
②年龄
随着年龄的增长,患皮肤癌的风险增加。这主要是由于累积的紫外线暴露和其他环境因素的影响。[13]
③个人或家族史
有皮肤癌个人或家族史的人风险更高。某些遗传性疾病也会增加皮肤癌的风险。[14]
④基因型
在基因型方面MC1R、IRF4、TP53等基因突变与角化细胞癌的发生也有很大关系。[15]
5.2预防
虽然不能完全消除皮肤癌的风险,但采取适当的预防措施可以显著降低患病几率。[3,4,16]关于皮肤癌的预防措施,大致可以分为以下几类:
1.日常防晒
①日常使用一个广谱防晒霜。
②使用防晒服、防紫外线太阳镜和宽边帽。
③尽可能寻找阴凉处,尤其是在上午10点到下午4点之间。
④为车窗和家中的窗户安装防紫外线膜。
⑤此外,在一项综述性文章中提到,国际非电离辐射防护委员会(ICNIRP)关于户外紫外线辐射防护的建议包括调整户外工作时间、设置遮阳结构,并在上午 11:00 至下午 3:00 之间尽可能在阴凉处工作。[3,4]
2.避免紫外线照射
①避免长时间晒太阳,防止晒伤,特别是对儿童。
②避免使用日光浴床。
③即使在阴天或冬季,也要采取防晒措施,因为紫外线可以穿透云层和衣物。
3.定期皮肤检查
①每月进行一次自我皮肤检查。
②每年至少看一次皮肤科医生进行专业检查。
③特别关注有痣或皮肤病变的区域。
4.提高意识
了解皮肤癌的风险因素和早期迹象,特别是如果有个人或家族病史。如果有任何皮肤上的异常变化,请及时咨询医疗专业人员。对皮肤癌预防相关知识的教育是预防皮肤癌的关键组成部分。由于紫外线辐射往往在年轻时开始,因此儿童和年轻人的防晒至关重要,因此加强这方面的教育是至关重要的。[17]总的来说,提高防范意识可以降低皮肤癌的发病率,但对皮肤癌发病率或死亡率的影响还是很有限的。
六、皮肤癌的治疗方案
皮肤癌的治疗方法取决于癌症的类型、大小、位置以及患者的整体健康状况。以下是皮肤癌的治疗一些常见的治疗方法:手术治疗、光动力治疗、放疗、药物治疗等。
6.1手术治疗
手术是治疗皮肤癌的常用手段。通过手术可以切除有癌症的皮肤,并让受影响的部位看起来更好。
①Mohs手术
对于某些类型的皮肤癌,特别是那些位于面部等敏感区域或复发的皮肤癌,Mohs手术是黄金标准。这种技术可以去除基底细胞癌,同时对健康组织的伤害最小,实现尽可能高的治愈率——首次治疗的肿瘤治愈率高达99%。
②常规手术
常规手术切除适用于早期、局限性皮肤癌,直接切除肿瘤及部分周围组织放射治疗。
6.2光动力治疗
光动力疗法(PDT)结合光能和局部光敏剂,这些光敏剂能产生细胞毒性的活性氧,对异常细胞具有肿瘤杀伤作用。光动力疗法清除皮肤癌的效率为 40%至 76.4%。[18]
6.3放疗
放射治疗使用高能量辐射杀死癌细胞或使其萎缩。对于不能手术切除的皮肤癌或手术后需要额外治疗的患者,放射治疗可能是一个有效的选择。
6.4药物治疗
对于非严重的基底细胞癌,可以使用外用药物治疗,如咪喹莫德和5-氟尿嘧啶。
6.5其他治疗
冷冻疗法(液氮冷冻)和电干燥法(电灼)适用于早期、小范围病变。
激光治疗:用于特定类型的皮肤癌。
以上方法常需结合使用,具体需由医生根据个体情况制定方案。更多细节可参考相关医疗指南或咨询专业医师。
七、总结
皮肤癌的防治关键在于早期发现与病因规避。
高危人群(如户外工作者、免疫抑制患者)需定期自检并结合专业筛查。
随着AI与无创技术的发展,未来诊断将更高效精准,为患者争取最佳治疗时机。
参考文献
- Hasan, N., Nadaf, A., Imran, M., Jiba, U., Sheikh, A., Almalki, W. H., Almujri, S. S., Mohammed, Y. H., Kesharwani, P., & Ahmad, F. J. (2023). Skin cancer: understanding the journey of transformation from conventional to advanced treatment approaches. Molecular cancer, 22(1), 168. https://doi.org/10.1186/s12943-023-01854-3
- Bray, F., Laversanne, M., Sung, H., Ferlay, J., Siegel, R. L., Soerjomataram, I., & Jemal, A. (2024). Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, 74(3), 229–263. https://doi.org/10.3322/caac.21834
- Perez, M., Abisaad, J. A., Rojas, K. D., Marchetti, M. A., & Jaimes, N. (2022). Skin cancer: Primary, secondary, and tertiary prevention. Part I. Journal of the American Academy of Dermatology, 87(2), 255–268. https://doi.org/10.1016/j.jaad.2021.12.066
- Rojas, K. D., Perez, M. E., Marchetti, M. A., Nichols, A. J., Penedo, F. J., & Jaimes, N. (2022). Skin cancer: Primary, secondary, and tertiary prevention. Part II. Journal of the American Academy of Dermatology, 87(2), 271–288. https://doi.org/10.1016/j.jaad.2022.01.053
- Gandini, S., Sera, F., Cattaruzza, M. S., Pasquini, P., Picconi, O., Boyle, P., & Melchi, C. F. (2005). Meta-analysis of risk factors for cutaneous melanoma: II. Sun exposure. European journal of cancer (Oxford, England : 1990), 41(1), 45–60. https://doi.org/10.1016/j.ejca.2004.10.016
- Gandini, S., Sera, F., Cattaruzza, M. S., Pasquini, P., Zanetti, R., Masini, C., Boyle, P., & Melchi, C. F. (2005). Meta-analysis of risk factors for cutaneous melanoma: III. Family history, actinic damage and phenotypic factors. European journal of cancer (Oxford, England : 1990), 41(14), 2040–2059. https://doi.org/10.1016/j.ejca.2005.03.034
- Green, A. C., & Olsen, C. M. (2015). Increased risk of melanoma in organ transplant recipients: systematic review and meta-analysis of cohort studies. Acta dermato-venereologica, 95(8), 923–927. https://doi.org/10.2340/00015555-2148
- Jensen, P., Møller, B., & Hansen, S. (2000). Skin cancer in kidney and heart transplant recipients and different long-term immunosuppressive therapy regimens. Journal of the American Academy of Dermatology, 42(2 Pt 1), 307. https://doi.org/10.1016/s0190-9622(00)90154-3
- Kuo, C. C., Moon, K. A., Wang, S. L., Silbergeld, E., & Navas-Acien, A. (2017). The Association of Arsenic Metabolism with Cancer, Cardiovascular Disease, and Diabetes: A Systematic Review of the Epidemiological Evidence. Environmental health perspectives, 125(8), 087001. https://doi.org/10.1289/EHP577
- Karagas, M. R., Gossai, A., Pierce, B., & Ahsan, H. (2015). Drinking Water Arsenic Contamination, Skin Lesions, and Malignancies: A Systematic Review of the Global Evidence. Current environmental health reports, 2(1), 52–68. https://doi.org/10.1007/s40572-014-0040-x
- Gamboa-Loira, B., Cebrián, M. E., Franco-Marina, F., & López-Carrillo, L. (2017). Arsenic metabolism and cancer risk: A meta-analysis. Environmental research, 156, 551–558. https://doi.org/10.1016/j.envres.2017.04.016
- Khalesi, M., Whiteman, D. C., Tran, B., Kimlin, M. G., Olsen, C. M., & Neale, R. E. (2013). A meta-analysis of pigmentary characteristics, sun sensitivity, freckling and melanocytic nevi and risk of basal cell carcinoma of the skin. Cancer epidemiology, 37(5), 534–543. https://doi.org/10.1016/j.canep.2013.05.008
- Bassukas, I. D., & Tatsioni, A. (2019). Male Sex is an Inherent Risk Factor for Basal Cell Carcinoma. Journal of skin cancer, 2019, 8304271. https://doi.org/10.1155/2019/8304271
- Gandini, S., Sera, F., Cattaruzza, M. S., Pasquini, P., Zanetti, R., Masini, C., Boyle, P., & Melchi, C. F. (2005). Meta-analysis of risk factors for cutaneous melanoma: III. Family history, actinic damage and phenotypic factors. European journal of cancer (Oxford, England : 1990), 41(14), 2040–2059. https://doi.org/10.1016/j.ejca.2005.03.034
- Choquet, H., Ashrafzadeh, S., Kim, Y., Asgari, M. M., & Jorgenson, E. (2020). Genetic and environmental factors underlying keratinocyte carcinoma risk. JCI insight, 5(10), e134783. https://doi.org/10.1172/jci.insight.134783
- Geisler, A. N., Austin, E., Nguyen, J., Hamzavi, I., Jagdeo, J., & Lim, H. W. (2021). Visible light. Part II: Photoprotection against visible and ultraviolet light. Journal of the American Academy of Dermatology, 84(5), 1233–1244. https://doi.org/10.1016/j.jaad.2020.11.074
- Hill, D., & Dixon, H. (1999). Promoting sun protection in children: rationale and challenges. Health education & behavior : the official publication of the Society for Public Health Education, 26(3), 409–417. https://doi.org/10.1177/109019819902600310
- Heppt, M. V., Steeb, T., Niesert, A. C., Zacher, M., Leiter, U., Garbe, C., & Berking, C. (2019). Local interventions for actinic keratosis in organ transplant recipients: a systematic review. The British journal of dermatology, 180(1), 43–50. https://doi.org/10.1111/bjd.17148


