
细胞外基质的稳定对组织结构和功能至关重要,而赖氨酰氧化酶(LOX/LOXL)家族正是维持这一稳定的关键催化酶。大量研究显示,LOX/LOXL在胶质瘤、乳腺癌、结直肠癌等多种恶性肿瘤中异常高表达,并与癌症的侵袭、转移及患者不良预后密切相关。然而,关于其转录调控机制、预后模型的优化以及在肿瘤免疫微环境中的作用,科学界仍知之甚少。
近日,首都医学科学创新中心高级研究员、北京朝阳医院血液科主任主鸿鹄教授团队徐擎昱主治医师与德国海德堡大学曼海姆医学院合作,在生物学领域重要期刊《Cell Communication and Signaling》(影响因子:8.2)上发表了最新研究成果。该研究题为“Machine learning-based in-silico analysis identifies signatures of lysyl oxidases for prognostic and therapeutic response prediction in cancer”,首次通过多组学数据与人工智能技术,系统评估了LOX/LOXL在33种癌症中的表达谱,深入揭示了其在肿瘤进展和免疫调控中的核心作用,为未来的靶向治疗和免疫治疗策略开辟了新路径。
研究亮点速览
多维数据整合,覆盖广泛
研究团队整合了来自TCGA、CGGA、GEO、CCLE等多个国际公共数据库的转录组数据,包括大样本RNA测序与单细胞RNA测序,样本量超过9000例,涵盖33种癌症类型,确保了分析广度与深度。
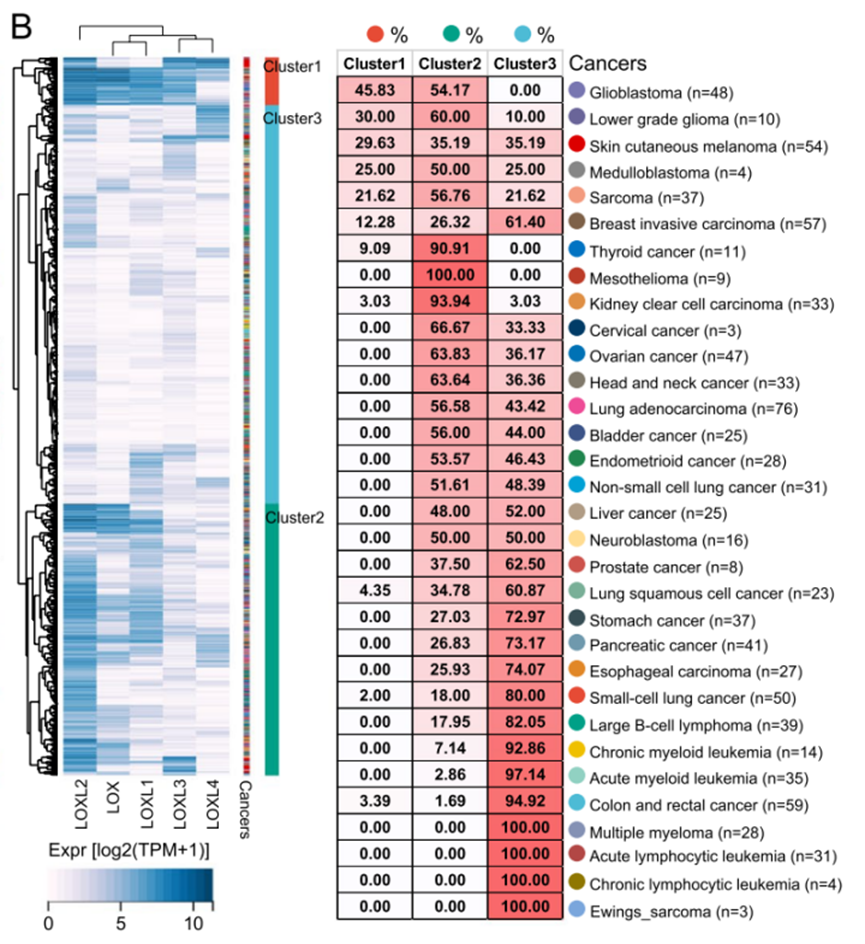
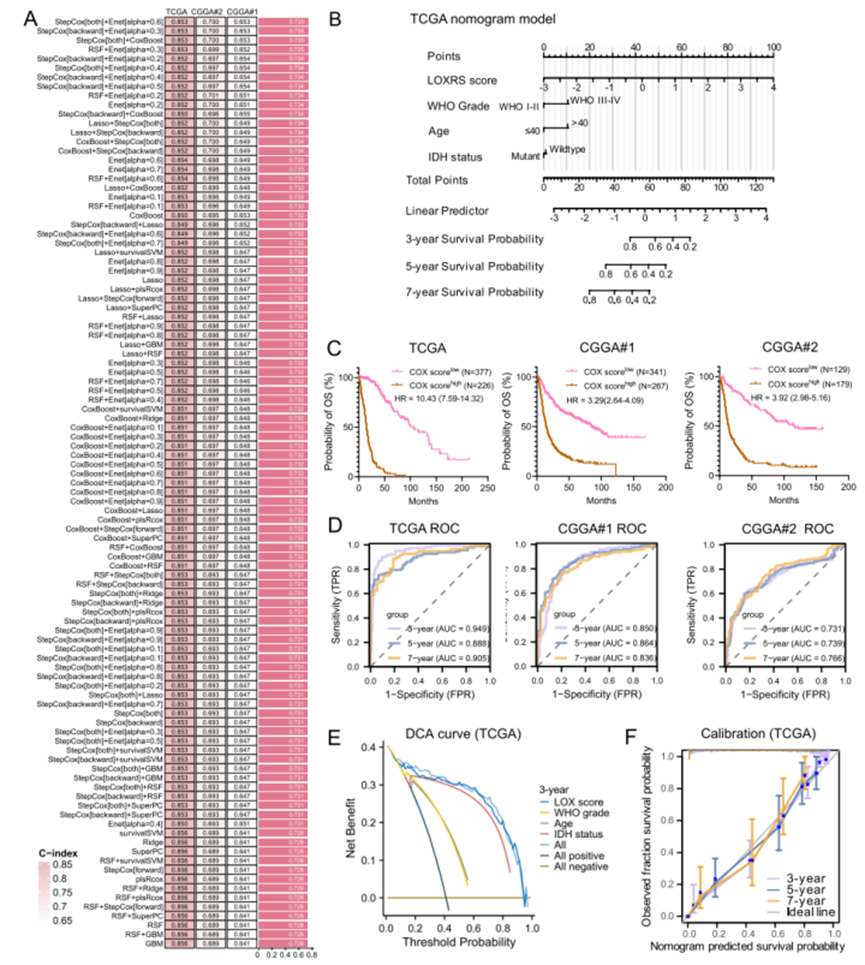
机器学习构建精准预后模型
通过10种机器学习算法组成的101种组合,研究人员筛选出21个与LOX/LOXL共表达的关键基因,并最终构建了一个包含12个基因的“LOX/LOXL相关标志物(LOXRS)”评分模型。该模型结合年龄、WHO分级、IDH突变状态等临床特征,能够准确预测胶质瘤患者的3年、5年及7年生存率(AUC值均大于0.73),为个体化治疗提供了可靠的决策工具。
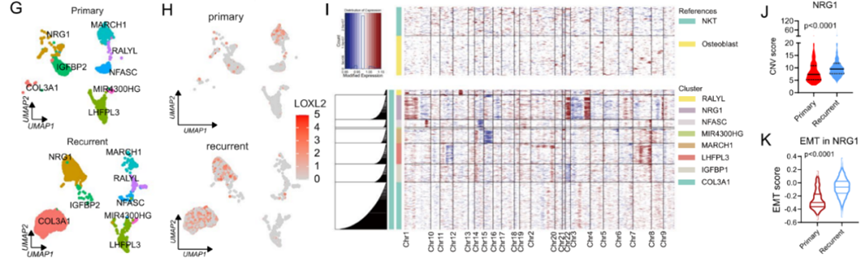
单细胞精度解析复发机制
在对IDH阴性胶质母细胞瘤的单细胞分析中发现,LOXL2在复发病例的特定恶性细胞亚群(如NRG1亚群)中特异性高表达,且与上皮-间质转化(EMT)和基因组不稳定性显著相关。这从单细胞层面揭示了LOX/LOXL家族驱动肿瘤复发的潜在新机制。
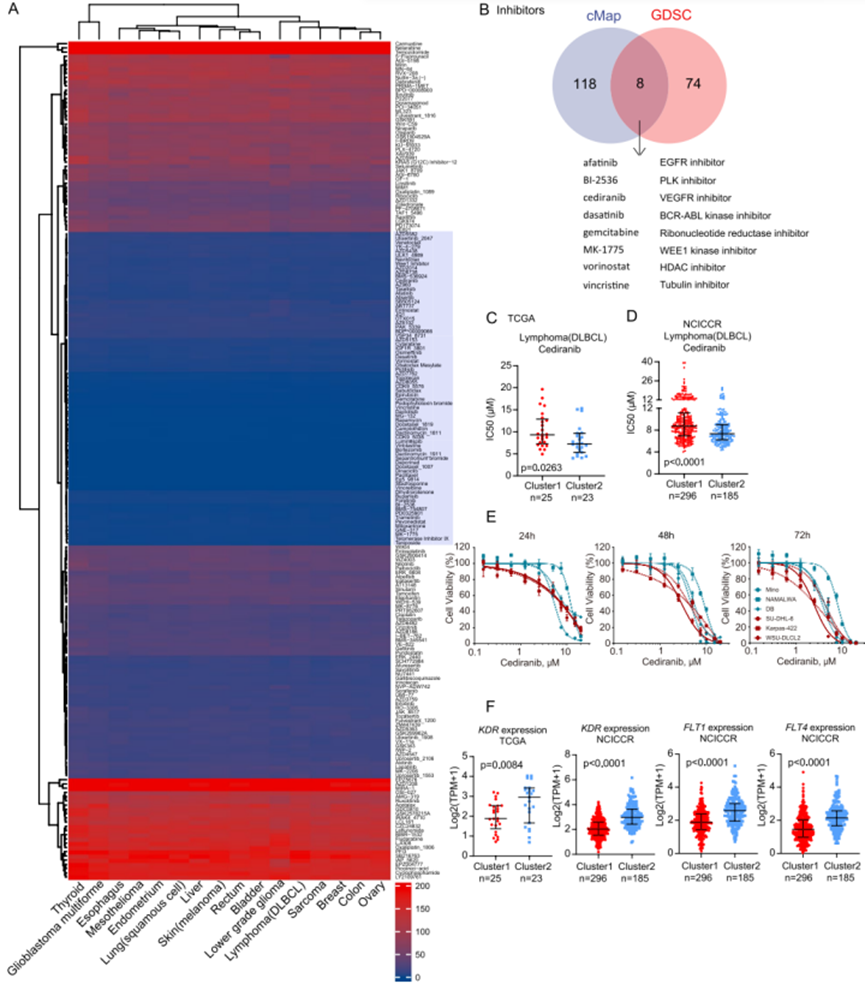
指向精准的药物预测与验证
利用Connectivity Map(cMap)数据库和oncoPredict等AI工具,研究筛选出可能靶向LOX/LOXL过表达癌细胞的潜在药物(如VEGFR抑制剂Cediranib)。后续的细胞实验证实,该药物在LOX/LOXL高表达的非霍奇金淋巴瘤细胞系中展现出显著疗效,为后续的临床试验奠定了理论基础。
预测免疫治疗响应
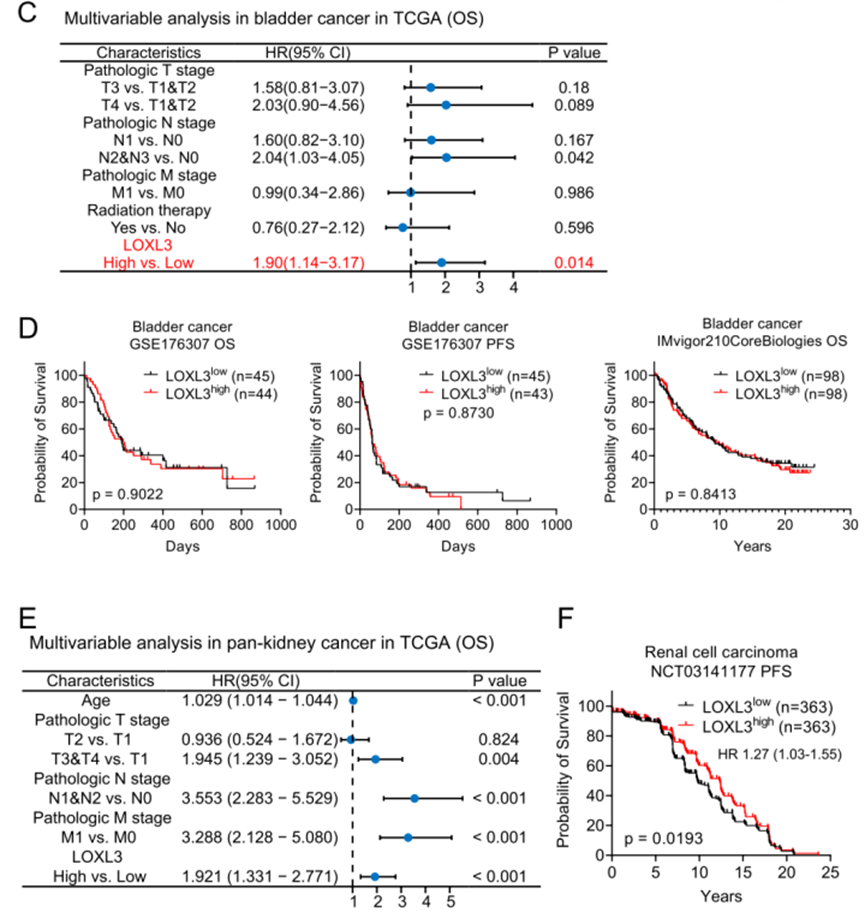
研究还发现,在肾癌和膀胱癌中,LOXL3的高表达与巨噬细胞等免疫细胞的浸润程度显著相关,并能预测患者对免疫检查点抑制剂(ICB)的治疗反应。这为免疫治疗的优势人群筛选提供了新的生物标志物。
总结与展望
本研究通过多组学整合与人工智能的方法,系统性地绘制了LOX/LOXL家族在泛癌中的功能图谱,不仅优化了癌症患者的预后预测体系,也为开发新的靶向治疗和免疫治疗联合策略提供了方向。
未来,研究人员计划通过动物模型及临床试验进一步验证所预测药物的疗效,并深入探索LOX/LOXL调控肿瘤微环境的具体分子机制,以期推动相关发现向临床精准治疗的转化。
文献来源:
Xu Q, Ma L, Streuer A, et al. Machine learning-based in-silico analysis identifies signatures of lysyl oxidases for prognostic and therapeutic response prediction in cancer. Cell Commun Signal (2025).
DOI: 10.1186/s12964-025-02176-1.


