白血病病因不明一直是国际白血病研究领域的痛点,推测外来因素导致了人造血干祖细胞基因突变最终导致了白血病的表型,但是尚无最直接证据来证实该推测。
2021年意大利学者首次报道了小细环病毒(TTMV)可整合至人视黄酸受体α(RARA)基因组位点,形成跨物种“病毒-宿主”融合基因TTMV::RARA,出现急性早幼粒细胞白血病表型。不仅突破了既往仅由“人-人”基因融合介导白血病的传统认知,也拓展了对AML发病机制的理解。然而,目前相关研究多局限于个案报道,导致TTMV的基因组插入特征、患者临床表现、分子遗传学基础及治疗策略均不明确,为临床诊疗带来严峻挑战。
近日,首都医学科学创新中心高级研究员、北京朝阳医院血液科主任主鸿鹄教授团队在《Haematologica》上发表题为 “The comprehensive landscape of TTMV::RARA fusion-driven acute myeloid leukemia: from viral integration mechanisms to clinical outcomes” 的研究论文。该研究系统揭示TTMV通过微同源介导末端连接机制特异性整合至人类基因组。此类患者以儿童为主,常伴有髓外病变及i(17)(q10)异常核型,并对全反式维甲酸(ATRA)联合砷剂(ATO)治疗具有较高敏感性,但仍面临高复发风险,提示造血干细胞移植可能作为潜在根治策略。该研究首次全面绘制了TTMV::RARA融合基因阳性白血病的临床-分子全景图谱,为该类罕见血液肿瘤的精准诊疗体系构建提供了关键依据。

【研究方法】
本研究共纳入2553例AML患者,通过整合病毒基因组数据的筛选流程,鉴定出10例TTMV::RARA融合基因阳性新发病例,结合已报道的15例患者,共同构成当前大规模的TTMV::RARA-AML患者的临床基因组数据集。研究系统采集了患者人口统计学资料、治疗方案(包括诱导/巩固化疗及造血干细胞移植)、分子遗传学特征以及全转录组(WTS)和全基因组(WGS)测序数据。所有患者均随访至2024年8月,研究终点严格遵循国际标准,包括完全缓解(CR)、总生存期(OS)、无事件生存期(EFS)和无复发生存期(RFS)。
【研究结果】
TTMV病毒整合特征
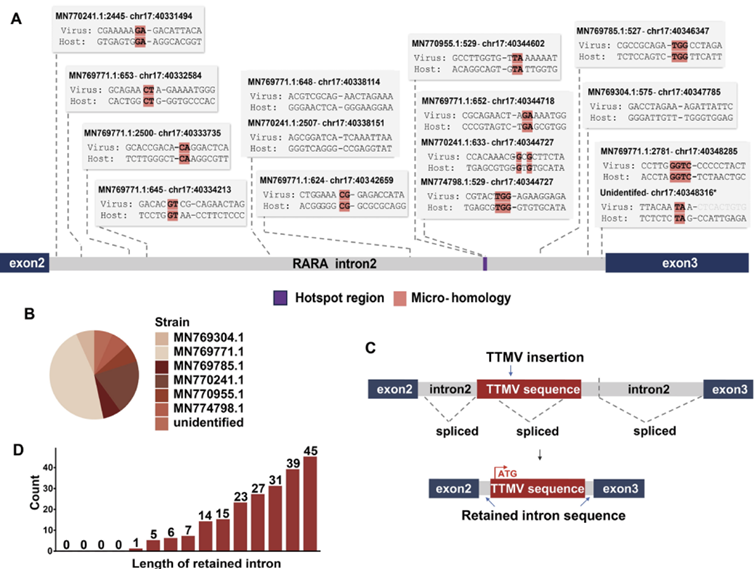
研究共鉴定出7种参与整合的TTMV病毒亚型,其中MN-769771.1为主要病毒株。所有病毒插入均精准定位于RARA基因的2号内含子区域,整合位点存在2–4 bp的微同源序列,提示该融合基因形成依赖于“微同源介导的末端连接”机制。进一步研究发现,病毒插入后首先形成RARA::TTMV::RARA前体转录本,随后通过可变剪接生成保留RARA完整开放阅读框的成熟致癌融合基因。
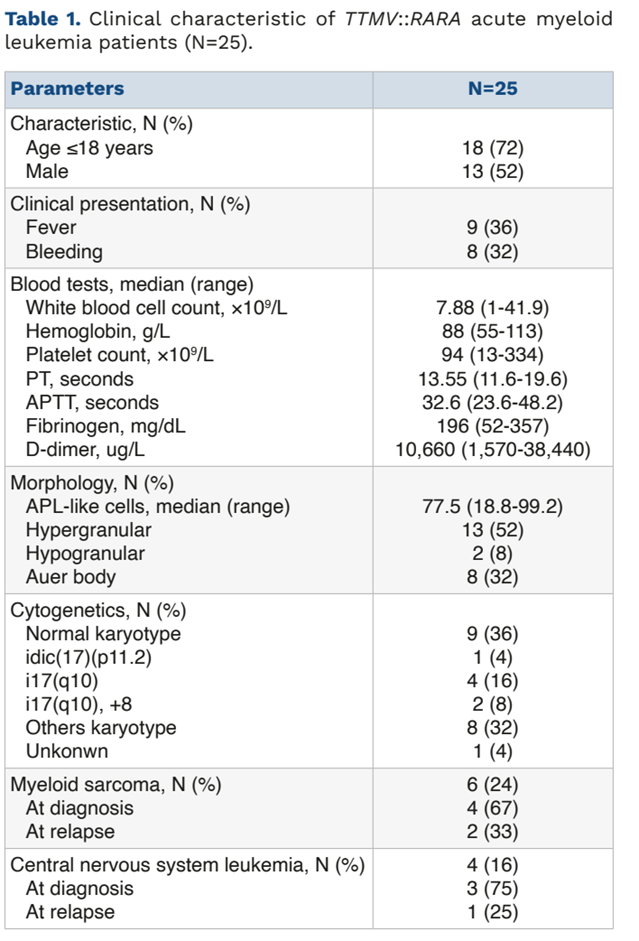
TTMV::RARA患者的基本特征
该类患者以儿童为主,常伴有较高比例的髓系肉瘤(24%)和中枢神经系统浸润(16%)等髓外浸润表现,提示其侵袭性更强。
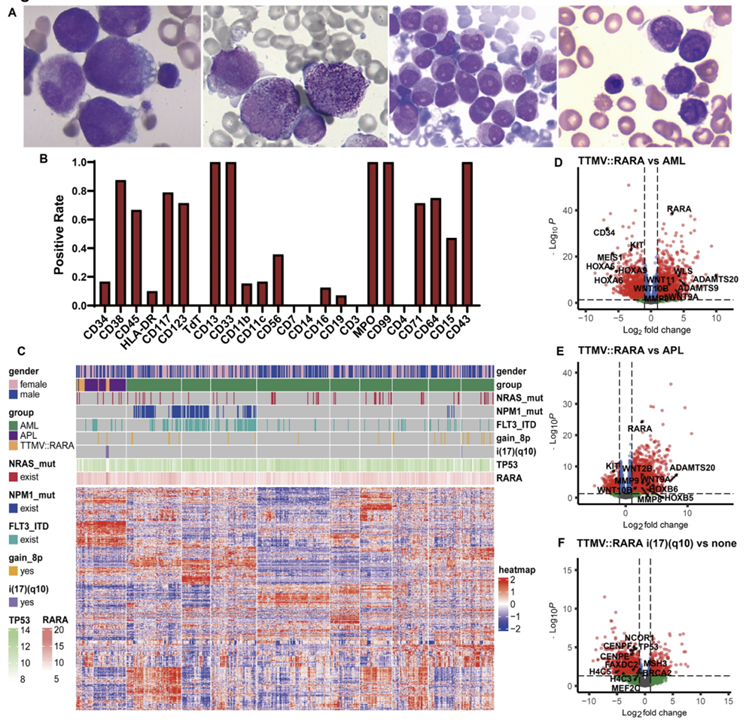
TTMV::RARA患者的MICM分型
进一步MICM特征分析显示,尽管TTMV::RARA-AML患者具备APL的形态学和免疫表型特征,但其遗传学及转录组表达谱与经典APL存在明显差异,并常伴随i(17)(q10)染色体异常。基于该异常可将患者进一步划分为两个分子亚群,为预后分层提供了依据。
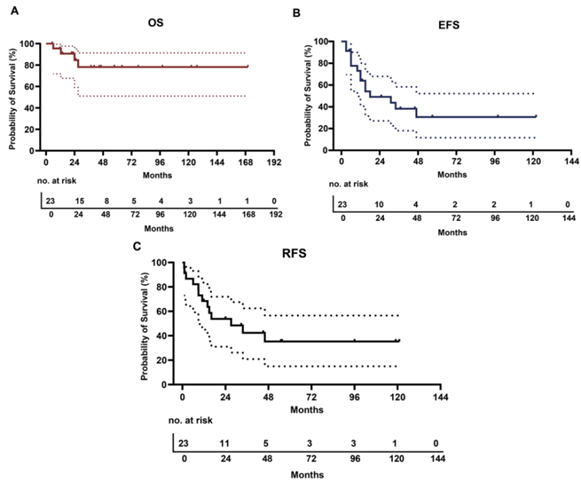
生存分析
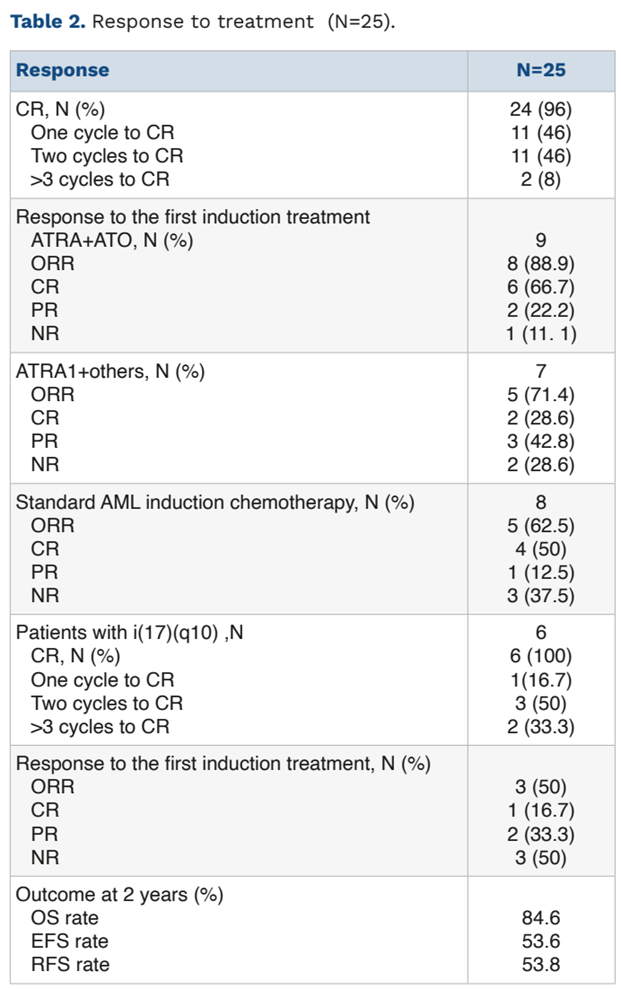
预后分析显示,患者2年总生存率为84.6%,且无早期死亡病例,但其突出临床挑战在于高复发风险。
临床治疗反应
在治疗方面,相较于其他方案,该类患者对全反式维甲酸(ATRA)联合砷剂(ATO)治疗表现出较高敏感性,且有望改善生存时间。然而,该方案仍难以有效遏制高复发风险。造血干细胞移植可能作为潜在根治策略:在接受移植的11例患者中,9例实现长期生存(中位随访时间36个月)。
【总结】
本研究首次系统阐明了“病毒-人”跨物种融合基因TTMV::RARA的基因组结构变异特征及其携带者的独特临床表现,从而将TTMV::RARA阳性白血病明确定义为一个全新的疾病实体。通过整合国际多中心合作的临床与多组学数据,不仅揭示了其在生物学行为上与经典RARA重排白血病的本质差异,也为构建该类型白血病的精准诊断、风险分层与靶向治疗体系提供了关键科学依据,具有重要的临床和科学价值,主鸿鹄教授实验室正在进行深入的机制研究,为该类罕见病的基础和临床转化研究提供更多数据,促进中国在该类白血病的研究领域处于国际领先地位。
【作者介绍】
本研究由主鸿鹄教授与浙江大学黄金艳教授担任共同通讯作者,首都医学科学创新中心Zhu Lab孙舒博士后、浙江大学刘永晶博士和北京朝阳医院的徐擎昱博士为共同第一作者。
【基金支持】
该研究工作获得了国家自然科学基金原创探索项目、面上项目、首都医学科学创新中心以及博士后特别资助等多个项目的支持。


